近日,山东大学微生物改造技术全国重点实验室高翔团队在肠道脆弱拟杆菌Ⅵ型分泌系统效应蛋白拮抗机制方面取得重要突破。相关研究成果以“A nonenzymatic effector disrupts Bacteroides cell wall homeostasis via OmpA targeting to mediate interbacterial competition”为题发表在综合期刊PNAS。山东大学微生物改造技术全国重点实验室博士生何静为论文第一作者,山东大学微生物改造技术全国重点实验室高翔为该研究的通讯作者。山东大学微生物改造技术全国重点实验室为第一完成单位和通讯作者单位。
人体胃肠道是生物密度最高的生态系统之一。作为这一环境中占据主导地位的革兰氏阴性菌,拟杆菌在维持肠道稳态中扮演着双重角色:一方面作为肠道共生菌,拟杆菌能够水解复杂多糖为宿主和其他微生物提供营养物质,另外一方面作为条件致病菌,拟杆菌还能够在宿主免疫受损时引起宿主多种感染。在革兰氏阴性菌的复杂斗争中,拟杆菌能够利用六型分泌系统与其他细菌争夺有限资源和生态位。然而,由于肠道拟杆菌培养的困难性、遗传操作的复杂性以及效应蛋白的独特性,导致目前对拟杆菌T6SS效应蛋白的了解非常有限。
在本研究中,高翔团队对肠道拟杆菌T6SS进行了系统的研究,在脆弱拟杆菌T6SS中鉴定出一种新型的效应蛋白BteO。综合运用细胞遗传学、生物化学、结构生物学及生物信息学等方法,作者逐步揭示了BteO独特的作用机制。该效应蛋白与多数已知效应蛋白通过酶解作用直接破坏细胞壁的方式不同,而是靶向结合敏感菌株的OmpAs外膜蛋白,干扰OmpAs与肽聚糖之间的稳定连接,破坏细胞壁的稳定性,从而逐步引发敏感菌株细胞伸长、鼓泡乃至裂解。并且该效应蛋白能够增强细菌在哺乳动物肠道中的竞争定殖能力。另外,肠道内丰富的胆盐能够显著增强BteO的菌间拮抗能力,这为理解肠道微生物在胁迫坏境下的适应性策略提供了新视角。该研究工作报道了一种通过非酶活机制破坏细菌细胞壁,驱动菌间拮抗的新机制。
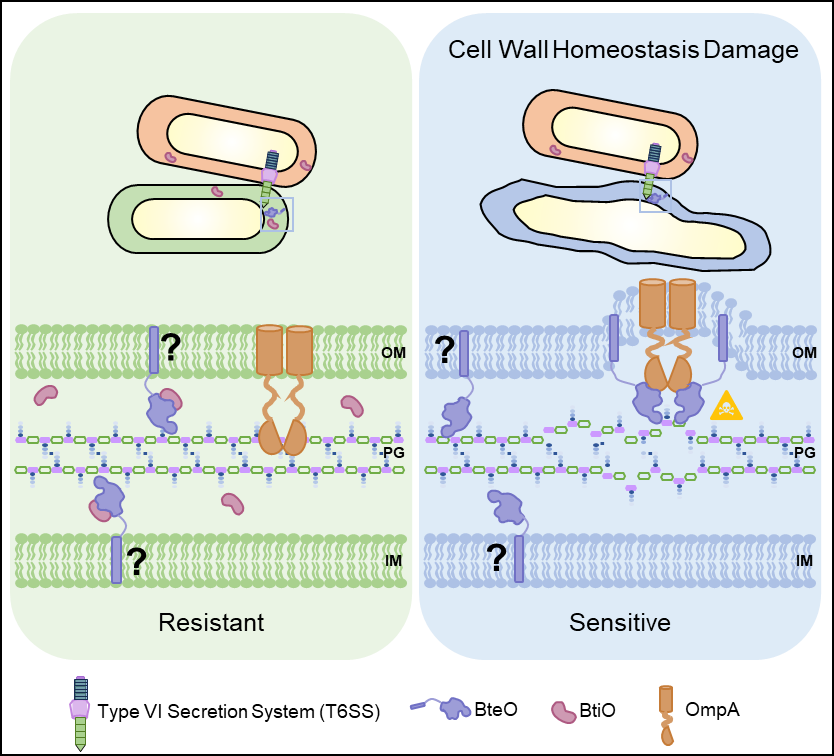
BteO作用机制的概述图
该研究工作得到了国家重点研发计划、国家自然科学基金、山东省自然科学基金、SKLMT前沿与挑战项目以及SKLMT内部联合项目基金等基金的资助。微生物改造技术全国重点实验室的刘双江教授与霍刘杰教授为本研究的顺利开展提供了重要的支持与协助。
文章链接:10.1073/pnas.2513207122.