2026年2月21日,山东大学微生物改造技术全国重点实验室高翔团队在Nature Communications上以长文形式在线发表题为Effector conformational plasticity enables lineage-specific secretion via Hcp heterohexamers in gut symbionts的研究文章,揭示了Hcp异源六聚体递送构象可塑性效应蛋白的分子机制。山东大学博士生郑帅宁、博士后李伟勋为论文共同第一作者,山东大学微生物改造技术全国重点实验室高翔教授为该研究的通讯作者。
人体肠道微生物是已知的最密集最多样化的微生物群落之一,其组成与人体健康密切相关。作为人体肠道最丰富的革兰氏阴性细菌,拟杆菌门在宿主的营养代谢、免疫调节以及肠道稳态维持中扮演关键角色。为了在菌间竞争中占据优势地位,肠道拟杆菌可借助接触依赖型VI分泌系统(Type VI secretion system, T6SS)以及非接触依赖型扩散性毒素,将其作为对抗其他拟杆菌的抗菌武器。
T6SS是革兰氏阴性细菌中广泛存在的一类接触依赖型分泌装置,在菌间竞争、维持微生物群落稳态等方面发挥重要作用。自2014年首次报道拟杆菌T6SS以来,已有研究鉴定出多种拟杆菌T6SS效应蛋白,这些效应蛋白包括干扰周质蛋白稳态、破坏外膜完整性以及协同降解细胞壁等多种毒性机制,揭示了拟杆菌T6SS效应蛋白在功能层面的多样性。然而,在递送机制层面,拟杆菌T6SS仍存在若干核心科学问题尚未解决。效应蛋白在供体菌中如何被特异性识别、精确装载并实现有序递送的分子机制,仍有待深入研究。
作为T6SS的核心结构蛋白,Hcp组装成六聚体环状结构,并堆叠组装形成中空管状结构,有研究表明Hcp约40 Å的内腔能够递送小分子量效应蛋白(< 20 kDa)。自2013年首次发现Hcp可与效应蛋白直接结合以来,尽管相关研究逐步深入,但Hcp如何特异性识别不同效应蛋白、效应蛋白以何种构象状态加载于Hcp管腔中,以及其递送过程中的结构动态变化等关键科学问题,尚不清楚。
与假单胞菌门(原变形菌门)每套T6SS基因簇编码单一Hcp蛋白不同,拟杆菌T6SS基因簇中编码至少5个Hcp同源蛋白。该研究表明在脆弱拟杆菌中5个Hcp同源蛋白的存在并非功能冗余,其中Hcp2和Hcp3必须组装成异源六聚体才能保持稳定,并特异性结合并递送V1区效应蛋白Bte1,而Hcp1作为5个Hcp中表达量最高的蛋白,其作为T6SS内管的主要组分,并不参与效应蛋白的结合,表明脆弱拟杆菌T6SS内管结构组装及效应蛋白装载存在明确的分工协作。
该研究进一步成功解析了Hcp2-Hcp3异源六聚体及其与效应蛋白Bte1形成的三元复合物的冷冻电镜结构,首次直观揭示了效应蛋白在Hcp内腔中的装载构象。结构分析显示,效应蛋白Bte1在装载过程中会发生显著的构象变化,以适应刚性的Hcp内管结构。这一结果表明,与以往认知不同,除分子量外,效应蛋白的构象可塑性也是决定其能否被装载入Hcp并实现递送的关键因素之一。进一步的系统发育分析及功能分析表明,在脆弱拟杆菌中,Hcp2-Hcp3异源六聚体与V1区效应蛋白形成了高度适配的共进化关系,其中,Hcp3内腔表面的序列不保守区域与效应蛋白结构保守但序列高度可变的N端结构域精准配对。
综上,该研究全面揭示了Hcp2/Hcp3异源六聚体特异性递送V1区效应蛋白的分子机制,证实了分子量较大的效应蛋白可通过构象变化适应狭窄Hcp内管进而被T6SS递送,突破了以往认为Hcp仅能递送较小分子量效应蛋白的观点,提出了Hcp变体与效应蛋白协同进化的“锁-钥”互作模型。该研究深化了对肠道菌群菌间竞争分子机制的理解,同时也为T6SS的工程化设计及潜在应用奠定了重要的结构及理论基础。
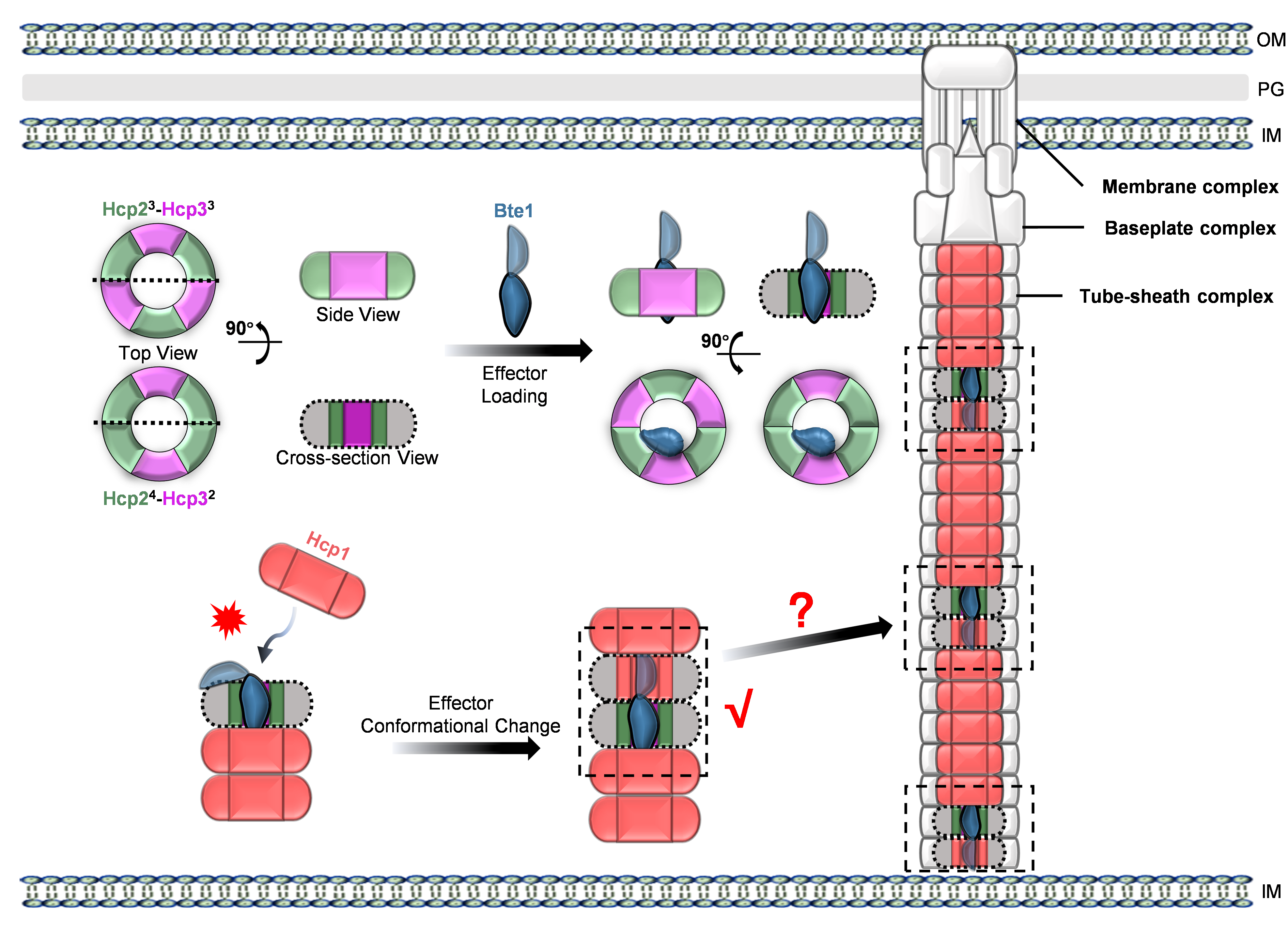
Hcp2-Hcp3异源六聚体递送V1区效应蛋白模式图